11 月 16 日,恒瑞医药宣布,其自主研发的 1 类新药 SHR-1314 获得 NMPA 核发的《药物临床试验批准通知书》,准许开展强直性脊柱炎适应症临床试验。

SHR-1314 注射液,即 Vunakizumab,是一款靶向人 IL-17A 的重组人源化单克隆抗体,拟用于治疗与 IL-17 通路相关的自身免疫疾病。Insight 数据库显示,这是该药获批的第二项临床,此前于 2016 年 6 月该药首次获批临床。目前,恒瑞已针对该药展开 7 项临床,最高处于临床 II 期。
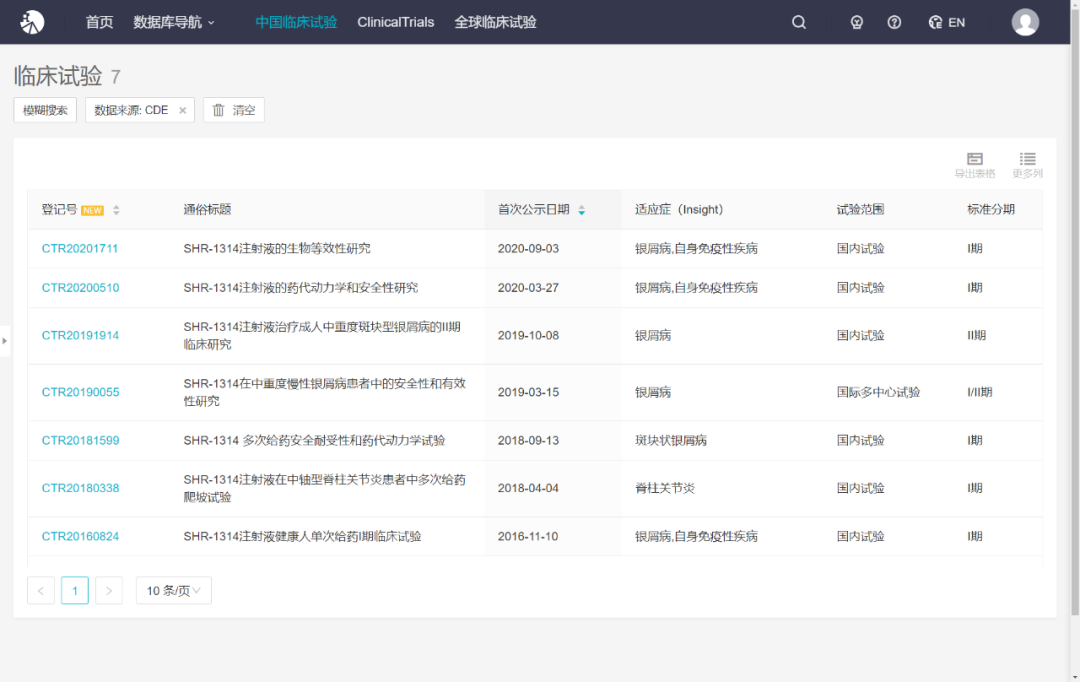
来自:Insight 数据库(http://db.dxy.cn/v5/home/)
目前全球已有 2 个 IL-17A 抗体获批上市。诺华公司的 secukinumab(商品名 Cosentyx)于 2015 年在美国和欧洲获批上市,2019 年其销售额为 35.51 亿美元;礼来公司的 ixekizumab(商品名 Taltz)于 2016 年在美国和欧洲获批上市,2019 年其销售额为 13.66 亿美元。Secukinumab 和 ixekizumab 分别于 2019 年 4 月和 9 月作为第一批临床急需境外新药在中国获批上市。
截至目前,该产品累计已投入研发费用约 17,119 万元人民币。

点击阅读原文
试用 Insight 数据库 30 天
本文来源:insight数据库 作者:小编 免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系
 insight数据库
insight数据库



 我们沟通的很顺畅
我们沟通的很顺畅 电话已拨通,无人接听
电话已拨通,无人接听 这个电话号码是空号
这个电话号码是空号