11 月 24 日,CDE 官网显示,豪森有两款仿制药上市申请获承办,分别为 3 类仿制药醋酸艾替班特注射液和地拉罗司片,目前两个品种国内均无企业获批。
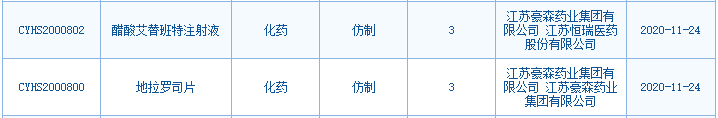
艾替班特注射液,原研全球销售额 20.6 亿元
艾替班特是武田旗下夏尔制药开发的一款高选择性缓激肽 B2 受体拮抗剂,主要用于治疗遗传性血管水肿(HAE)急性发作。HAE 是一种罕见的遗传性疾病,发病时的主要表现为反复发生的皮肤、呼吸道和内脏器官肿胀,当水肿发生于气道时,可致喉水肿,如果抢救不及时,可窒息死亡。
艾替班特在 2011 年获得 FDA 批准上市(商品名:Firazyr),用于 18 岁及以上成年人的遗传性血管水肿急性发作治疗,成为 FDA 批准的第 3 个用于治疗遗传性血管水肿发作的药物。
据武田财报显示,2019 年 Firazyr 全球销售额 327 亿日元(约合人民币 20.6亿元),同比增长 409%。在国内,武田制药早在今年 6 月 11 日递交醋酸艾替班特注射液上市申请,后又纳入优先审评,预计最快明年有望获批。
目前,国内布局艾替班特注射液仿制药的企业除豪森外还有成都圣诺在 2018 年已报上市,但值得注意的是,豪森的艾替班特注射液已于今年 3 月份获 FDA 批准,这意味着豪森有望凭借国内外共线生产加速在国内的上市速度。

地拉罗司片,原研全球销售额达 9.75 亿美元
地拉罗司是 FDA 在 2005 年批准的第一个能够常规使用的口服铁螯合剂,目前已在 80 多个国家上市。在美国上市的口服混悬液和分散片,被批准用于治疗 2 岁及以上的成年和小儿患者因输血而引起的慢性铁过载,和 10 岁以上非输血依赖性地中海贫血(NTDT)综合征患者的慢性铁过载。
2010 年,地拉罗司分散片在中国获批上市,用于因需要长期输血而引致铁质积聚的患者(如患有地中海贫血症或其他罕见的贫血症) ,适用于两岁以上儿童及成人服用。目前国内暂无普通片剂获批,但是分散片已有 3 家仿制药递交上市申请。
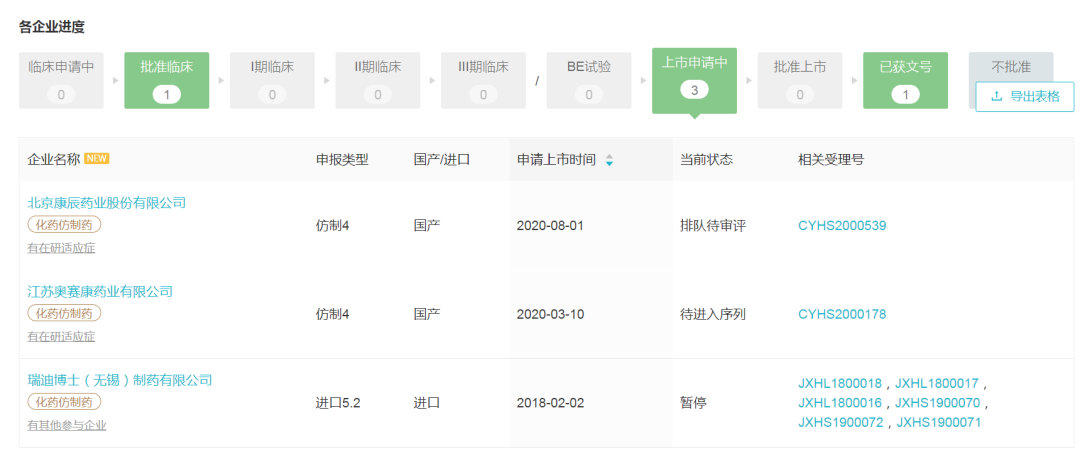
据诺华2019 年财报显示,地拉罗司全球销售额达 9.75 亿美元;国内 2019 年地拉罗司分散片通过国家谈判进入了最新版医保目录;公开数据显示,2019 年前三季度地拉罗司国内销售额为 700.29 万元。

点击阅读原文
申请数据库试用 30 天
本文来源:insight数据库 作者:微微阳 免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系
 insight数据库
insight数据库



 我们沟通的很顺畅
我们沟通的很顺畅 电话已拨通,无人接听
电话已拨通,无人接听 这个电话号码是空号
这个电话号码是空号