精彩内容
日前,成都圣诺生物以仿制4类申报的依替巴肽注射液(受理号CYHS1700193)获批生产并视同过评,为国内首家。米内网数据显示,该产品在2019年中国公立医疗机构终端增速超过200%。
依替巴肽是血小板糖蛋白Ⅱb/Ⅲa受体拮抗剂,
图1:2015-2019年中国公立医疗机构终端依替巴肽注射液销售情况(单位:亿元)
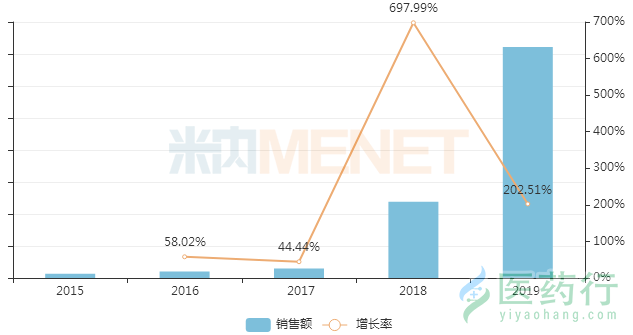
来源:米内网中国公立医疗机构终端竞争格局
米内网数据显示,依替巴肽注射液在2019年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端增速超过200%,目前由豪森主导市场。
图2:依替巴肽注射液一致性评价开展情况(含新分类报产)
来源:米内网一致性评价数据库
目前仅深圳翰宇药业提交依替巴肽注射液一致性评价补充申请,还在审评审批中;5家企业以新分类报产,其中成都圣诺生物的产品已获批生产并视同过评,为国内首家。
本文来源:米内网 作者:君臣佐使 免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系
 米内网
米内网



 我们沟通的很顺畅
我们沟通的很顺畅 电话已拨通,无人接听
电话已拨通,无人接听 这个电话号码是空号
这个电话号码是空号