瑞德西韦仿制药印度获批,定价39-78美元,总治疗成本低至195美元!
编译丨newborn 今年5月,吉利德抗病毒药物瑞德西韦(remdesivir)获得日本厚生劳动省(MHLW)批准,成为全球第一个被批准用于治疗COVID-19的药物。此外,该药已在全球多个国家和地区被授予紧急使用授权或扩大同期用药,包括美国、英国、欧盟。 6月21日,印度...
文/Linan
投稿邮箱:yiyao@yidu.sinanet.com
◆ ◆ ◆
6月22日,君实生物发布首次公开发行股票并在科创板上市招股意向书。根据招股意向书,君实生物计划发行8713万股A股于科创板上市,公开发行股份数量占本次发行后总股本的10%,将于6月29日初步询价确定A股发行价。君实生物曾在2015年8月在新三板挂牌并公开转让。2018年12月,君实生物再发行H股登陆港交所。如今君实生物又将目光瞄向了科创板,采用第五套上市标准,拟募资27亿元。
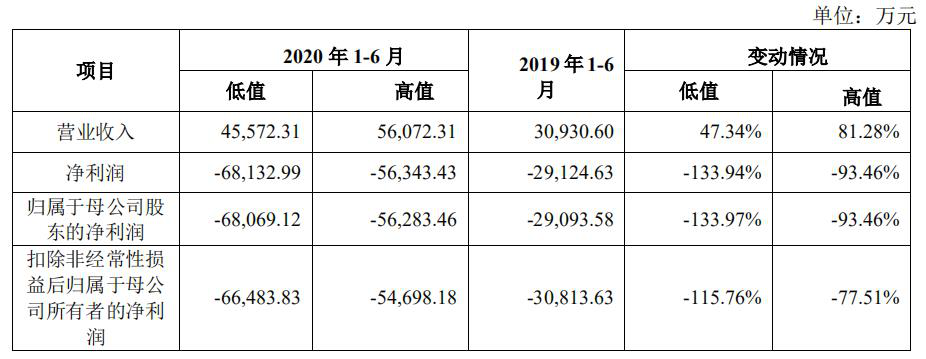
特瑞普利单抗注射液(商品名:拓益)是君实生物的唯一的上市销售药物,也是其收入和利润的主要来源。君实2019年年报显示,全年实现营业收入7.75亿元,较2018年的93.4万元实现突飞式增长,同比增长828.86倍。特瑞普利销售收入占其营业务收入的99.999%。2019年,该产品销售收入达到7.74亿元,销售毛利率为88.3%。君实的特瑞普利单抗注射液于2018年12月17日获NMPA有条件批准上市,是国内首个获批上市的国产PD-1单克隆抗体注射液,用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。此后,信达、恒瑞、百济神州的PD-1产品相继获批,目前中国市场上一共有六款针对PD-1靶点的产品,此外还有15款处于临床或上市申请阶段。根据弗若斯特沙利文的预测,到2030年,我国PD-1/PD-L1抑制剂的市场规模将达到988亿元。在PD-1在研管线中,各药企的竞争日趋激烈。
直播丨22日19:30,聊聊肿瘤免疫治疗新突破--双特异性抗体疗法
近几年医药行业政策不断推出,一致性评价、中国加入ICH、MAH落实、药物临床试验数据核查等加速行业优胜劣汰;医疗、医保、医药联动,加速医疗改革;行业格局将加速重塑。在医疗政策改革的推动下,我国医药产业的发展正步入规范的快车道。在“健康中国”上升为...
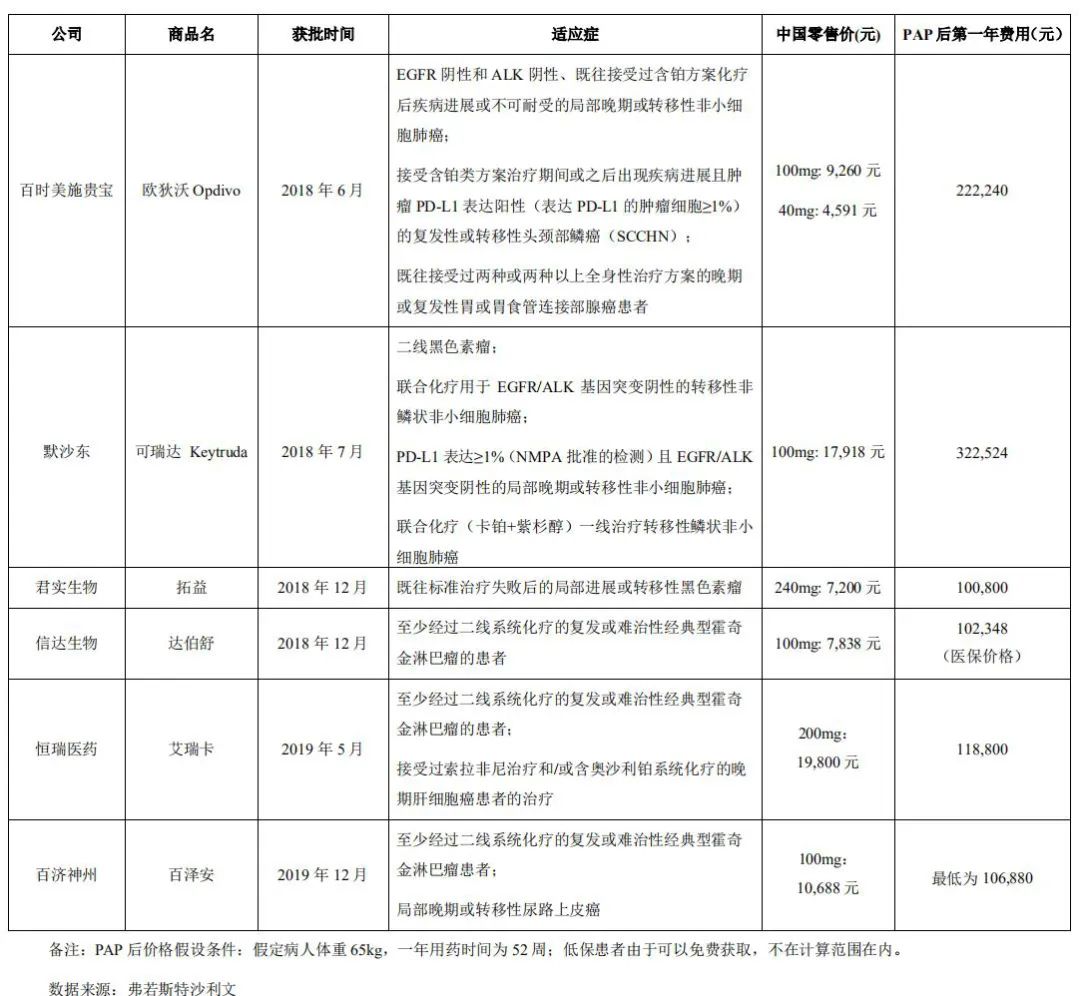
(点击查看大图)
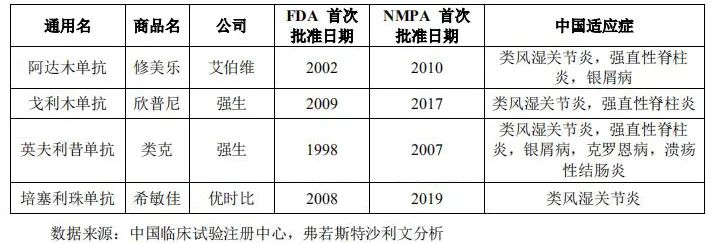
君实的阿达木单抗生物类似药为12项在研抗TNF-u单抗中第三个提交NDA的产品。阿达木生物类似药竞品较多,且受原研药降价影响定价水平较低,市场竞争较为激烈。另外,君实JS002(重组人源化抗PCSK9单抗注射液)正在开展临床Ⅱ期试验,虽然君实核心产品具有较大的市场空间,但同时也面临着较大的市场竞争,并且其一部分产品临床试验排名未处于市场第一梯队,后续业绩如何也有待观察。但是对于君实来说,在当前持续亏损下,扭亏转盈压力还是很大的。君实方面提到,如果上市后未能实现盈利,按照科创板的规则,可能会面临终止上市的风险。(注:相关资料参考自君实生物招股意向书)
END
相关阅读
疫情逼停,中国船员滞留海外邮轮上百日!从加勒比海到英吉利海峡,他们经历了什么?
文/haon 投稿邮箱:yiyao@yidu.sinanet.com ◆ ◆ ◆ “ 中国的疫情防控已经打完了上半场,但世界还有很多角落在经历着下半场。 看似光鲜靓丽的“海上城堡”,在新冠疫情期间,却成了一个个飘零零、危险重重的孤岛。 随着钻石公主号、赞丹号、威士特丹号、...
本文来源:新浪医药 作者:Linan 免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系
 新浪医药
新浪医药





 我们沟通的很顺畅
我们沟通的很顺畅 电话已拨通,无人接听
电话已拨通,无人接听 这个电话号码是空号
这个电话号码是空号