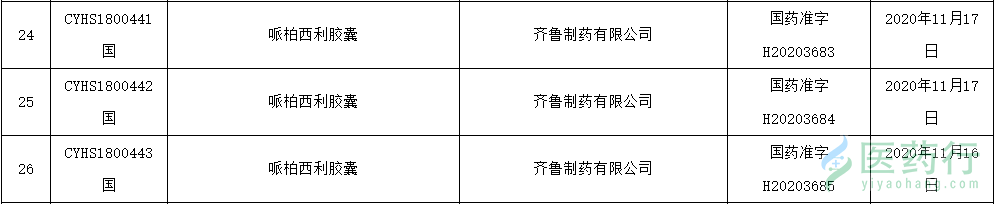
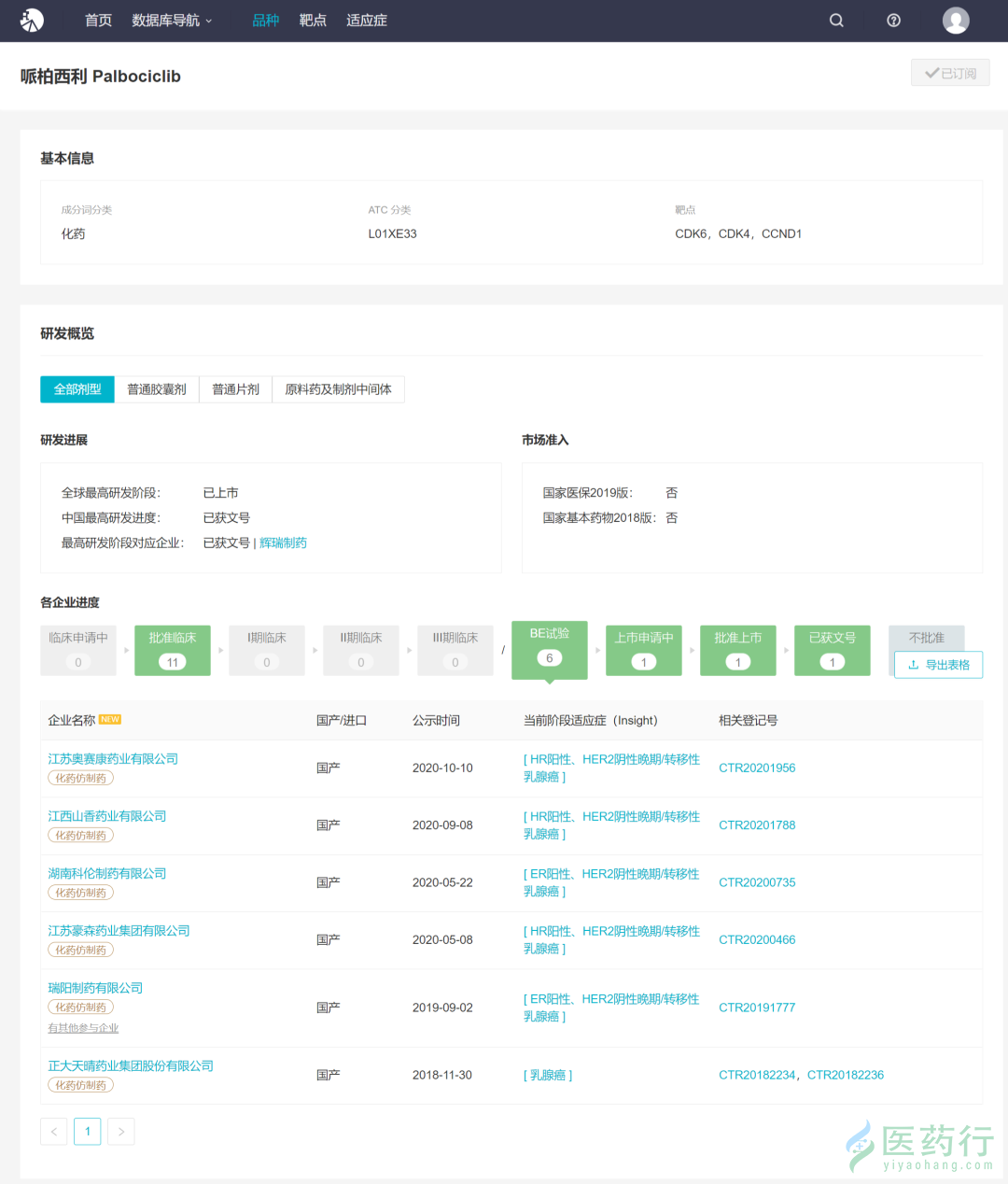
12 月 18 日,NMPA 发布批件,齐鲁制药 4 类仿制药「哌柏西利胶囊」获批上市 ,为该品种国内首仿。其适应症为:一线联合芳香化酶抑制剂治疗绝经后女性、激素受体阳性(HR+)、人表皮生长因子受体 2 阴性(HER2-)局部晚期或转移性的乳腺癌。 哌柏西利(palbociclib)最早由辉瑞研发, 是全球首个上市的 CDK 4/6 抑制剂。 2015 年 2 月,哌柏西利通过加快审评途径获美国 FDA 批准上市(商品名:Ibrance),用于与来曲唑联合作为初始内分泌疗法治疗 HR+/HER2- 的晚期乳腺癌 。 目前,Ibrance 已在欧盟、 日本等多个国家和地区上市。 该品种是当之无愧的重磅品种,自上市以来,其全球销售额连年增长,至 2019 年其年销售额已达 49.61 亿美元(+20.47%)。 2018 年 7 月,原研哌柏西利首次在中国获批,商品名为爱博新,用于联用芳香化酶抑制剂作为初始内分泌疗法治疗 HR+/HER2- 局部晚期或转移性乳腺癌。 当前,除原研辉瑞外,已有 19 家企业布局其仿制药,其中先声药业已于今年 3 月报产,奥赛康、豪森、科伦、正大天晴等 6 家企业正在 BE 试验阶段,另有 11 家企业获批临床。 来自 I nsight 数据库(http://db.dxy.cn/v5/home/) 目前,在全球范围内,已有三款 CDK4/6 抑制剂获批,分别为辉瑞的 palbociclib(哌柏西利)、诺华的 Ribociclib 和礼来的 Abemaciclib。然而,除了辉瑞哌柏西利之外,尚未有其他 CDK4/6 抑制剂在国内获批,仅礼来 Abemaciclib 片于 2019 年 11 月报产。 本次齐鲁的哌柏西利仿制药获批,意味着国内迎来首个国产 CDK4/6 抑制剂,乳腺癌患者将迎来新的治疗选择。
另外,CDK4/6 靶点在国内也是热门的在研靶点。同靶点新药已有 11 家国内企业处于临床阶段,涉及复星医药、豪森、正大天晴等,其中恒瑞的 SHR6390 进度最快,11 月 17 日,SHR6390 联合内分泌治疗在 HR 阳性、HER2 阴性女性乳腺癌的辅助治疗的国际多中心、随机、双盲的 Ⅲ 期临床试验获批,预计即将启动。
本文来源:insight数据库 作者:Insight数据库
免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系

 insight数据库
2020-12-18 00:00
1335
insight数据库
2020-12-18 00:00
1335



