今日(1月25日),国家药监局发布《关于修订吉非替尼片说明书的公告》,对吉非替尼片说明书【不良反应】、【注意事项】项进行修订。 从修订内容来看,此次主要涉及皮肤方面的问题,比如在【不良反应】中要求增加 皮肤和皮下组织异常等不良反应。 而【注意事项】要求增加严重皮肤不良反应(NCI CTCAE 3级或3级以上)需暂停用药,对皮肤反应进行早期干预有利于吉非替尼的持续治疗。患者用药期间出现皮肤感觉异常等应及时就医等相关内容。(具体见文末附件)


《通知》要求所有吉非替尼片生产企业均应依据《药品注册管理办法》等有关规定,按照吉非替尼片说明书修订要求,提出修订说明书的补充申请,于2021年4月20日前报国家局药品审批中心或省级药品监管部门备案。 修订内容涉及药品标签的,应当一并进行修订;说明书及标签其他内容应当与原批准内容一致。在补充申请备案后9个月内对所有已出厂的药品说明书及标签予以更换。 吉非替尼片生产企业应当对新增不良反应发生机制开展深入研究,采取有效措施做好使用和安全性问题的宣传培训,涉及用药安全的内容变更要立即以适当方式通知药品经营和使用单位,指导医师、药师合理用药。
关于吉非替尼
吉非替尼是一种选择性表皮生长因子受体酪氨酸激酶抑制剂,适用于表皮生长因子受体基因具有敏感突变的局部晚期或转移性非小细胞肺癌患者的一线治疗,及适用于治疗既往接受过化学治疗的局部晚期或转移性非小细胞肺癌患者。 吉非替尼直接抑制肿瘤生成的靶点,使肿瘤细胞特异性死亡而不波及正常细胞组织;与传统化疗药物相比,吉非替尼在取得抗肿瘤疗效的同时较少引起患者全身性副反应。此外,吉非替尼片是口服剂,接受其治疗的患者无须住院给药,这很大程度上提高了患者及其家属的生活质量。
吉非替尼临床应用广泛,目前已被《NCCN非小细胞肺癌临床实践指南(2020.V1)》、《中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南(2019)》等指南推荐作为EGFR突变非小细胞肺癌患者的一线治疗药物,且已进入2019年国家乙类医保和2018年国家基药目录。 吉非替尼2002年7月在日本首次上市,2003年5月获FDA批准在美国上市,2005年,原研药企阿斯利康的吉非替尼片(易瑞沙)在国内上市,并保持国内市场垄断长达11年之久,价格始终高达5000元/盒。
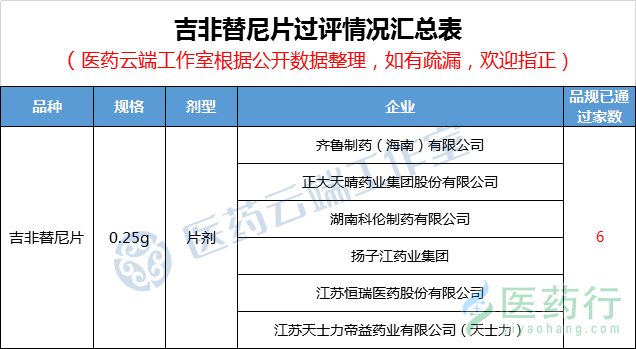
根据医药云端工作室统计,截止目前,该药品已6家企业过评,加上原研企业阿斯利康,七强争霸赛开启。
另据Insight 数据库显示,目前还有南京优科、上海创诺、苏州特瑞等多家企业的仿制药在报上市,其中包括 NATCO 制药公司的进口仿制药,竞争可谓异常激烈。
据米内网数据显示,2018年中国公立医疗机构终端吉非替尼的销售额超过23亿元。目前市场的领军企业为阿斯利康,不过齐鲁制药(海南)的产品至获批上市后一直蚕食原研的份额。 2019阿斯利康市场下降至74.96%,齐鲁制药的市场增长至23.56%,而正大天晴夺得1.48%的市场份额。 在4+7集采中,阿斯利康的吉非替尼片(250mg*10片)以547元中选,降幅为76%,要知道,这一价格是在2016年国家卫计委谈判中55%降幅的基础上再次降价的,使得同组的齐鲁在4+7集采中失利。 阿斯利康这一超低价也打破了业界对外资药企不愿降价或小幅降价的固有概念。 2019年9月,联盟地区药品集采中,阿斯利康、正大天晴和齐鲁制药的吉非替尼片分别以54.7元/片、45元/片和25.7元/片的价格中标。 不过,在“4+7”续签工作中,正大天晴和齐鲁制药在成都和福建等地区顶替阿斯利康拿下吉非替尼片中选资格。 另外值得关注的是,在2020年7月, 广东省药学会发布了《超药品说明书用药目录(2020年版)》, 230个药品可以超说明书使用,吉非替尼就榜上有名。药品被允许进行超说明书使用,可以说又增加了一些市场机会。而此次说明书修订会对它带来什么影响,我们拭目以待。
吉非替尼片上市后观察到以下不良反应。这些不良反应来自于无法确定样本量的自发报告,难以准确估计其发生频率。 皮肤和皮下组织异常:皮肤不良反应是吉非替尼片十分常见的不良反应之一,可发生在身体任何部位,多表现为轻到中度的皮疹、干燥、瘙痒等。上市后不良反应监测已收到掌跖红肿综合征(手足综合征、手足皮肤反应)报告,表现为手掌和足底感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度等。 皮肤毒性:严重皮肤不良反应(NCI CTCAE 3级或3级以上)需暂停用药(见【用法用量】),对皮肤反应进行早期干预有利于吉非替尼的持续治疗。患者用药期间出现皮肤感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度应及时就医。 上市后不良反应监测已收到掌跖红肿综合征(手足综合征、手足皮肤反应)报告,患者在用药期间应注意减少皮肤压迫和摩擦,尤其防止对手掌和足底的压迫。 (注:说明书其他内容如与上述修订要求不一致的,应当一并进行修订。)
本文来源:医药云端工作室 作者:小编
免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系



 医药云端工作室
2021-01-26 06:32
1060
医药云端工作室
2021-01-26 06:32
1060


